El 2, 3 difosfoglicerato (2, 3 DPG) es un compuesto derivado de un producto intermedio de la glucólisis; se concentra particularmente en el nivel de eritrocitos, ya que los glóbulos rojos, al carecer de mitocondrias, aprovechan el metabolismo del ácido láctico anaeróbico (fermentación homoláctica de la glucosa) para obtener energía.
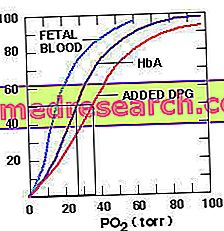
La hemoglobina es una proteína tetramérica que consta de cuatro subunidades, dos alfa y dos beta, cada una compuesta de una porción de proteína (globina) y una EME (grupo protésico de unión al oxígeno). El 2, 3-difosfoglicerato se adhiere a las cadenas Beta al compactarlas y reducir la afinidad de la hemoglobina por el oxígeno.
La unión de 2, 3 DPG a la hemoglobina ocurre cuando está en forma desoxigenada, mientras que se disuelve a nivel pulmonar por la unión de la hemoglobina con el oxígeno. De hecho, cuando la hemoglobina llega a los tejidos, las cadenas β son las primeras en liberar el oxígeno y esta pérdida conduce a un desplazamiento de los monómeros del centro. Tan pronto como se abre la cavidad hidrofílica interna, el DPG entra y se une al tetrámero, formando enlaces heteropolares entre sus grupos cargados negativamente y los residuos de lisina e histidina de las cadenas Beta, cargados positivamente. La estructura así estabilizada también puede liberar el oxígeno de las dos cadenas α. En los pulmones, sin embargo, tiene lugar el proceso inverso; a alta presión de oxígeno, las cadenas α son las primeras en unirse y el DPG se "exprime" y se expulsa del tetrámero, lo que permite un enlace β de la cadena de oxígeno más fácil.
El 2, 3 bisfosfoglicerato no puede unirse a la hemoglobina fetal, ya que esta molécula carece de las cadenas B con las que se une el 2, 3 DPG. Esto explica la mayor afinidad por el oxígeno de la hemoglobina fetal en comparación con la materna, una característica que permite que la sangre fetal extraiga oxígeno de la sangre materna.